衰老是机体不可避免的过程,具体表现在细胞和器官层面上的衰竭和患病风险的上升。作为衰老过程中重要的分子特征,转录组的改变成为各个器官功能衰退的分子标志物。lncRNA有较强的组织和物种特异性,而衰老相关的lncRNA则具有更强的进化保守性[1]。今天小编就借两篇安诺基因合作文章,和大家聊一聊lncRNA如何参与衰老调控~
文献一:lncRNA促进骨衰老[2]

发表时间:2021年3月
发表期刊:Theranostics(IF 8.575)
合作单位:西北工业大学
材料选择
小鼠模型(18月龄C57BL/6小鼠 vs 6月龄对照组小鼠);细胞模型(小鼠模型原代骨髓间充质骨祖细胞的lnc-PMIF敲降/过表达细胞系)。
提供服务:lncRNA测序
主要研究内容
老年小鼠骨形成减少伴随着骨髓间充质干细胞的迁移能力降低,长链非编码RNA PMIF在老年小鼠的骨髓间充质干细胞中表达上调,并导致老年OPCs向骨形成表面迁移能力降低。
机制上,lncRNA-PMIF可以与HuR蛋白结合,阻断HuR与β-actin mRNA的结合作用,抑制β-actin的表达,从而抑制老年OPCs的迁移。
研究者鉴定到一个人类lnc-PMIF同源基因,它是从人类Macf1基因位点转录而来的另一个转录本。敲降lnc-PMIF可以直接抑制体外人源成骨前体细胞hFOB1.19的迁移活性。
在转化医学方面,本研究揭示了以lnc-PMIF为靶点促进老年OPCs向骨形成表面迁移可能是一种全新的老年骨质疏松合成代谢策略。
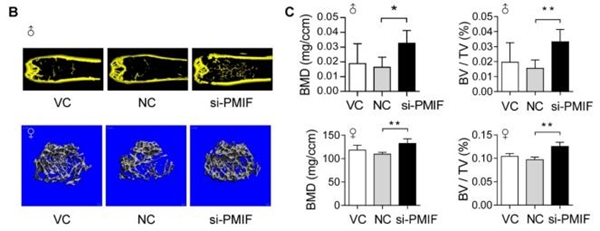
图1 lnc-PMIF在小鼠骨衰老过程中扮演重要角色
文献二:转录组测序鉴定参与小鼠老年性耳聋调控的lncRNA[3]

发表时间:2020年4月
发表期刊:Aging(IF 4.830)
合作单位:滨州医学院
材料选择
动物模型(6周龄 C57BL16J小鼠耳蜗 vs 1岁小鼠耳蜗);
细胞模型。
提供服务:lncRNA测序分析
主要研究内容
年龄相关的听力损失(AHL)是老年人群的重要健康问题。其分子机制尚未完全阐明。
本研究通过lncRNA测序分析鉴定了6周龄和1岁C57BL16J小鼠耳蜗中差异表达的mRNA和lncRNA,锁定34个和听力损失相关的基因,并且通过mRNA-lncRNA共表达网络确定11个lncRNA对上述基因具有调节作用。
在动物模型和细胞模型中对11个可以调控听力损失的lncRNA进行qPCR验证,确定候选lncRNA:NONMMUT010961.2。
在细胞模型中敲降NONMMUT010961.2后,Ar基因(控制氧化应激和凋亡)和Hgf基因(听力损失)的表达显著降低。表明lncRNA NONMMUT010961.2可能与AHL有关,为AHL治疗提供了新的思路。
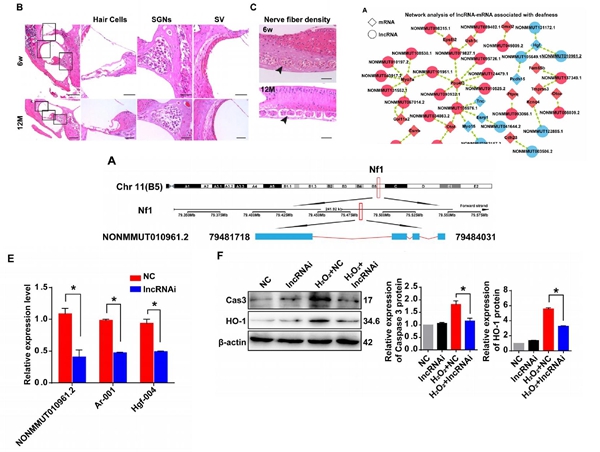
图2 lncRNA NONMMUT010961.2参与AHL进展
参考文献:
[1] Donghong Cai & Jing-Dong J. Han. Aging-associated lncRNAs are evolutionarily conserved and participate in NFκB signaling[J]. Nature Aging, 2021, 5.
[2] Targeting long noncoding RNA PMIF facilitates osteo-progenitor cells migrating to bone formation surface to promote bone formation during aging[J]. Theranostics, 2021,3
[3] Zhao T, Liu X, Sun Z, et al. RNA-seq analysis of potential lncRNAs for age-related hearing loss in a mouse model[J]. Aging (Albany NY), 2020, 12(8).


